Leukämie
"Wir wollen fehlerhafte Signale abschalten"
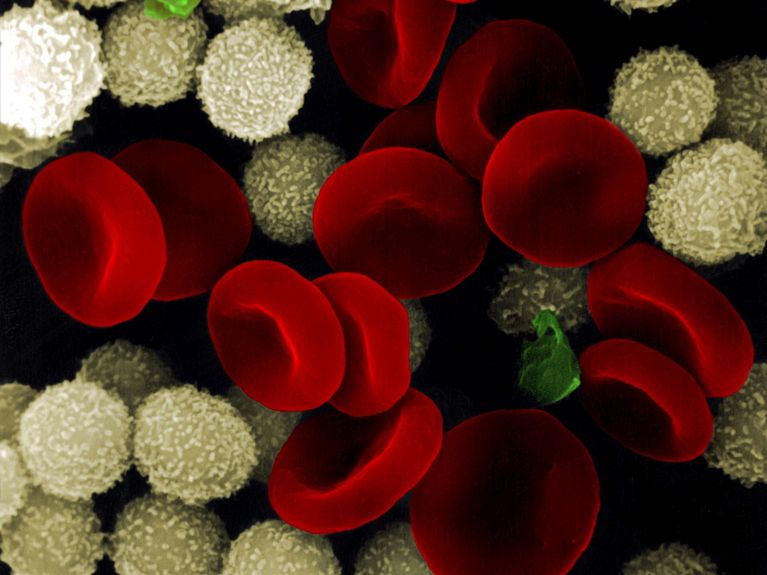
Falsches Signal. Bei Leukämiepatienten löst ein Gendefekt die übermäßige Produktion weißer Blutkörperchen aus. Bild: OKAPIA KG, Germany
Medikamente können die Symptome von Leukämie lindern, doch häufig verschlechtert sich die Krankheit trotzdem. Der Forscher Achim Leutz über fehlgesteuerte Mechanismen beim Blutkrebs
Herr Leutz, Sie untersuchen zelluläre Prozesse, die bei Leukämie eine Rolle spielen. Gegen die Krankheit gibt es doch schon Medikamente, warum also noch weiter forschen?
Weil bisherige Medikamente vor allem die Krankheitssymptome bekämpfen, aber nicht die wirkliche Ursache. Wir haben nun herausgefunden, warum sich Blutkrebs trotz laufender Behandlung verschlimmern kann. Dabei haben wir speziell die chronisch myeloische Leukämie, die CML, untersucht, die etwa jeden zehnten Fall von Blutkrebs ausmacht.
Was genau passiert bei dieser Krankheit?
Charakteristisch für die CML ist, dass sich die weißen Blutkörperchen unkontrolliert vermehren. Das liegt am veränderten Erbgut einer Blutstammzelle: Teile zweier Chromosomen verschmelzen zum so genannten Philadelphia-Chromosom. Dies ist Bestandteil eines Tumorgens - und dessen Produkt, ein spezielles Protein, ist wiederum für die verstärkte Bildung von weißen Blutkörperchen verantwortlich. Das Tumorprotein produziert Signale, die es in dieser Form eigentlich nicht geben sollte. Sie werden von der Zelle als Wachstumssignale interpretiert, blockieren aber auch die Zellreifung und die Wachstumskontrolle.
Mit anderen Worten: Diese Zellen wachsen zu einem Tumor heran?
Genau. Einige dieser Zusammenhänge sind bereits seit Ende der 1960er Jahre bekannt und in den 1980er Jahren wurden die molekularen Grundlagen dazu entdeckt. Seit 2002 ist auch ein Wirkstoff im Einsatz, das Imatinib, das das Tumorprotein hemmt und die Signalweiterleitung stoppt. Der erste überragende Erfolg der molekularen Therapien.
Achim Leutz ist am Max-Delbrück-Centrum für Molekulare Medizin (MDC) Berlin-Buch spezialisiert auf Zelldifferenzierung und Tumorentstehung. Außerdem ist er Professor für Molekulare Entwicklungsbiologie und Onkologie an der Humboldt-Universität Berlin. Bild: MDC / David Ausserhofer
Das klingt doch sehr gut, wo ist denn dann das Problem?
Imatinib und ähnliche Hemmstoffe verhindern, dass sich die Tumorstammzellen vermehren - und damit auch, dass das leukämische Krankheitsbild voranschreitet. Was sie aber nicht unterdrücken, ist die Aktivität der Zelle, die an der Leukämie Schuld hat. Die Patienten werden zwar die Symptome los, aber nicht die Krankheit. Das ist immerhin schon ein sehr großer Fortschritt, doch die Krankheit kann sich weiter entwickeln, wenn diese Tumorstammzelle weiter mutiert. Sie kann dann eine lebensbedrohliche Blastenkrise auslösen.
Was passiert bei so einer Blastenkrise?
Das Blut wird mit unreifen weißen Blutzellen überschwemmt, den Blasten. Medikamente helfen hier meist nicht mehr. Die große Frage ist also: Wie kommt man an die Tumorstammzelle heran? Wie kann man bereits die fehlerhafte Stammzelle identifizieren und nicht erst ihr Produkt? Denn Tumorstammzellen haben ähnliche Eigenschaften wie andere Stammzellen auch, sie tragen ja keine 'Tumorfähnchen'...
An welcher Stelle in diesen Prozessen setzt Ihre Forschung an?
Wir haben uns zwei Signalwege angesehen: Zum einen den so genannten Wnt-Signalweg, dessen Hauptbestandteil das Protein beta-Catenin ist. Er steuert normalerweise embryonale Zellen und die Geweberegeneration - wird er fälschlich aktiviert, können verschiedene Krebserkrankungen entstehen. Forschungen haben gezeigt, dass bei einer Blastenkrise sehr häufig das beta-Catenin aktiviert ist. Und dass anzunehmen ist, dass dieser Signalweg den leukämischen Zustand aufrechterhält. Zum anderen gibt es den Interferon-Signalweg. Der so genannte Interferon-regulatorische Faktor 8, Irf8, schützt vor Infektionen und reguliert die Entstehung bestimmter weißer Blutkörperchen, der neutrophilen Granulozyten. Irf8 sagt den Zellen, in welche Richtung sie sich spezialisieren sollen. Er wirkt aber auch dem Tumorprotein entgegen und kann so die Krebsentstehung unterdrücken.
Und was haben Sie herausgefunden?
Unsere früheren Arbeiten hatten gezeigt, dass das beta-Catenin in entwickelten Blutstammzellen keine weitere Rolle spielt, bei Leukämie jedoch hochreguliert ist. So kam uns die Idee: Wenn man das Gen eliminieren könnte, das beta-Catenin entstehen lässt, wäre das möglicherweise eine Korrektur für solche leukämischen Zellen. Wir haben dann anhand von Mäusen, denen Irf8 fehlt, gesehen, dass wir durch eine verstärkte Aktivierung des zuständigen Wnt-Signalwegs eine Blastenkrise auslösen können. Zudem haben wir gezeigt, dass die Blockade von Irf8 und die Aktivierung von beta-Catenin dafür verantwortlich sind, dass Medikamente wie Imatinib gegen die Tumorstammzellen wirkungslos sind.
Sind dies also die beiden Stellschrauben, mit denen sich die Krankheit in Schach halten lässt?
Genau. Daraus ergibt sich die Überlegung, auch beim Menschen nach Möglichkeiten zu suchen, in Tumorstammzellen Irf8 vermehrt zu aktivieren und das beta-Catenin auszuschalten, das ja in normalen Blutstammzellen nicht gebraucht wird, wie unsere frühere Arbeit zeigte. Schon in der Vergangenheit wurden Patienten erfolgreich mit Interferon Alpha behandelt, das die Hochregulation von Ifr8 bewirkt. Einige konnten auch ursächlich geheilt werden. Das Problem ist aber, dass die Behandlung mit Interferon sehr viele Nebenwirkungen hat. Darum sind Alternativen gefragt, vielleicht eben auch solche, die das beta-Catenin ausschalten. Oder eine Kombinationstherapie, die Ifr8 hochreguliert und beta-Catenin blockiert. Doch bevor wir zu große Hoffnung säen, müssen unsere Ergebnisse klinisch verifiziert werden.
Leser:innenkommentare