Interview
Jede einzelne Zelle im Blick
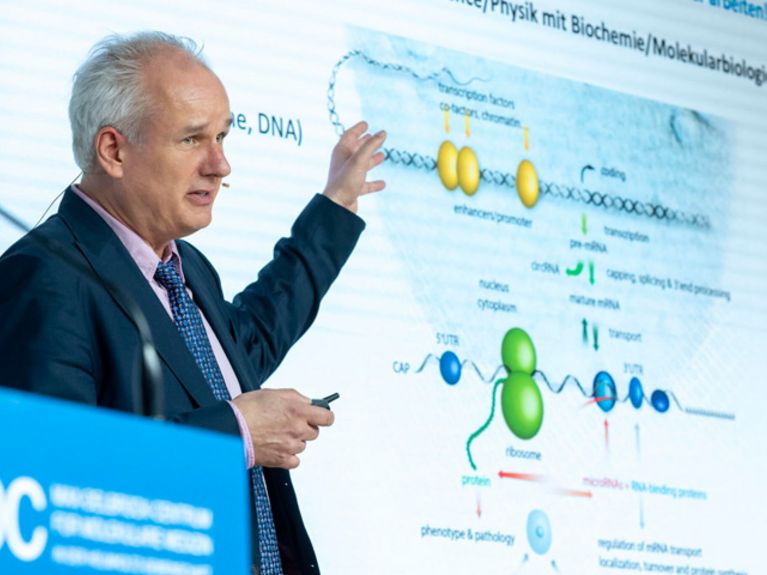
Nikolaus Rajewsky koordiniert gemeinsam mit Geneviève Almouzni vom Institut Curie in Paris die LifeTime-Initiative, an der rund 120 Wissenschaftler aus 18 Ländern beteiligt sind. Bild: David Ausserhofer/MDC
Wie kann man bei jeder Zelle im Körper kontrollieren, ob sie sich gesund entwickelt oder krank wird? Die Initiative "LifeTime" kombiniert dafür künstliche Intelligenz und Molekularbiologie.
Organe im Mini-Format In der Petrischale gezüchtete menschliche Mini-Organe (Organoide) ermöglichen personalisierte Krankheitsmodelle. Sie können zeigen, wie die Zellen wachsen, sich regenerieren und welche Veränderungen zu Krankheiten führen. Bild: A. Rybak Wolf/MDC
Herr Rajewsky, die Fachzeitschrift „Science“ hat die Methoden von LifeTime zum „Wissenschaftsdurchbruch des Jahres 2018“ erklärt. Worum geht es Ihnen?
Letztlich wollen wir mit LifeTime langfristig die gesamte Gesundheitsversorgung verbessern. Schlüssel dazu sind die Zellen, die Einheit des menschlichen Lebens. Wir haben heute die Möglichkeit, in sie hineinzuschauen: Wie trifft die Zelle Entscheidungen? Was passiert, wenn sie krank wird? Wir wollen Zellen beobachten und gezielt eingreifen, wenn sie von einer gesunden Entwicklung abweichen. Ich habe überhaupt keinen Zweifel daran, dass wir mit unserer Arbeit medizinischen Fortschritt erzielen werden.
Mit Zellen beschäftigen sich Forscher schon lange. Was ist das Besondere an Ihrem Ansatz?
Wir integrieren neue und sehr junge Methoden, um Krankheiten auf die Spur zu kommen. Das ist für mich so begeisternd! Beim Kartieren der Zellen, wie wir es nennen, geht es zunächst um eine Analyse einzelner Zellen und ihrer Strukturen und darum, welche Proteine ihre Gene herstellen. Um das herauszufinden, nutzen wir besonders effiziente Einzelzellanalysen – die sogenannten "single-cell multi-omics" – sowie bildgebende Verfahren. Möglich werden die Analysen der Datensätze erst durch maschinelles Lernen und künstliche Intelligenz. Und wir studieren Organoide, also 3D-Miniaturnachbildungen von Organen, die aus Hautzellen von Patienten entwickelt werden.
Welche Krankheiten haben Sie im Blick?
Uns geht es natürlich weniger um Knochenbruch – auch wenn die Regeneration sicherlich interessant wäre. Uns geht es um die großen Killer, also komplexe Erkrankungen wie Krebs, wo die Vielzahl unterschiedlicher Varianten ein enormes Problem ist, oder neurodegenerative Krankheiten oder Herz-Kreislauf-Erkrankungen. Dazu kommen die seltenen Erkrankungen – die sind zwar selten, aber von ihnen gibt es viele. Und Infektionskrankheiten wie Grippe oder Hepatitis.
Forschung trifft auf moderne Architektur. Das Muster des neuen BIMSB-Gebäudes in Berlin-Mitte erinnert an Pflanzenranken oder DNA-Stränge und reflektiert Sonnenlicht. Bild: Noshe
Wo setzen Sie mit der Forschung hier konkret an?
Uns geht es um molekulare Mechanismen: Zellen verändern sich ja im Krankheitsverlauf, und wir wollen genau wissen, warum und wie die einzelne Zelle das tut. Mit der CRISPR-Cas9-Methode, manchmal auch Genschere genannt, wollen wir dann etwa testen, ob ein bestimmter Abschnitt im Genom tatsächlich eine Krankheit verursacht, wie wir vermuten – und das Ganze, ohne dabei einen Patienten belasten zu müssen. Ich nenne diesen Schritt gerne "das Differenzial zwischen gesund und krank verstehen". Nur so können wir eines Tages Veränderungen auch vorhersagen und medizinisch eingreifen. Wir wollen nicht nur erkennen, wann eine Zelle vom gesunden Muster abweicht, sondern sie auch wieder in die richtigen Bahnen lenken.
Sie bringen in der Initiative Forscherinnen und Forscher aus ganz Europa zusammen …
…und aus ganz verschiedenen Disziplinen, genau. Ich bin überzeugt, dass wir wirkliche Veränderungen in der Gesundheitsversorgung nur dann bewirken können, wenn wir Experten aus unterschiedlichen Fachrichtungen zusammenbringen – und das tun wir. Ich glaube fest daran, dass das hier nicht nur akademisch interessante Wege sind, sondern dass am Ende Produkte stehen werden, die den Menschen wirklich helfen können. Deshalb stehen wir schon jetzt mit den Praktikern im engen Austausch, schließlich geht es uns um die Anwendung.
Noch steht die Initiative am Anfang. Wie realistisch ist ein Erfolg?
Das ist ungefähr so, als würde man Herrn Röntgen fragen, ob er glaube, mit dem Röntgenbild medizinische Fortschritte erzielen zu können. Der hätte auch nicht gezweifelt. Unsere Methoden sind so viel sensitiver als frühere Ansätze und geben so viel mehr Informationen auf der molekularen Ebene preis, dass wir ganz klar bessere Diagnosen werden stellen können. Wir werden neue Angriffspunkte finden, über die wir Krankheiten besser in den Griff bekommen. Lapidar gesagt: Angaben zum Blutdruck oder zur Temperatur reichen bei molekularen Krankheiten wie Alzheimer einfach nicht aus. Für mich ist tiefes Verstehen der einzige Schritt zum Heilen. Da unterscheiden wir uns von anderen Initiativen.
Sie spielen damit auf ein anderes Großforschungsprojekt an, an dem Sie auch beteiligt sind: den Human Cell Atlas.
Ja, bei dieser Initiative geht es darum, die Zelltypen im menschlichen Körper molekular zu erfassen. Bei LifeTime wollen wir mehr: Wir befassen uns mit dem Lebensverlauf von Zellen bei fortschreitenden Krankheiten. Auch methodisch gibt es Unterschiede, wir legen zum Beispiel den größeren Schwerpunkt auf maschinelles Lernen und künstliche Intelligenz. Uns verbindet dennoch vieles, und fast alle europäischen Partner sind auch an der US-Initiative Human Cell Atlas beteiligt.
Braucht es dann wirklich beide Initiativen?
Alleine das Vorhaben des Human Cell Atlas ist gewaltig und unseres noch mal mehr. Das lässt sich nicht zusammenfassen. Außerdem halte ich es für wichtig, dass wir in Europa den Patienten helfen und Verbesserungen in der Medizin anstreben, das können Sie nicht in die USA auslagern. Die Steuerungsgruppe des Human Cell Atlas sieht das übrigens genauso und unterstützt uns (und umgekehrt).
Wie ist bei LifeTime aus der Idee die große Forschungsinitiative geworden?
Die für LifeTime so wichtige Methode der Einzelzellanalysen machen wir ja hier am neuen Berliner Institut für Medizinische Systembiologie (BIMSB) des Max-Delbrück-Centrums – da lag es nahe, noch mehr rausholen zu wollen. Ich habe darüber lange nachgedacht und an einem Wochenende die entscheidenden fünf Seiten zur Vision aufgeschrieben (lacht). Aber im Ernst: Natürlich habe ich viel mit sehr guten Kollegen diskutiert. So sind noch andere Aspekte wie etwa die Epigenetik ins Konsortium gekommen, aber die Vision ist immer noch die gleiche.
Was braucht es, um diese inhaltliche Vielfalt zusammenzuhalten?
Wir sind zusammengekommen, weil wir hinter einem gemeinsamen Ziel stehen. Das zu spüren, ist etwas ganz Tolles. Wir können es auch nur zusammen erreichen. Dafür brauchen wir natürlich Fördergelder, auch europäische.
Und organisatorisch?
Ich versuche, intensiv mit den Beteiligten zu sprechen, immer für das Konsortium da zu sein. Und dann gibt es natürlich die Kernpartner aus den verschiedenen Ländern, die dort LifeTime umsetzen. Mit ihnen ist der Austausch besonders eng, teils treffen wir Entscheidungen gemeinsam. Häufig ist meine Rolle einfach, die Diskussion voranzutreiben.
Sie haben gerade erst als Direktor das BIMSB eröffnet – wie finden Sie da überhaupt noch Zeit für die LifeTime-Initiative?
Als Ausgleich spiele ich leidenschaftlich gerne Klavier, ohne das ginge es nicht. Sie haben natürlich recht. Die Arbeitstage sind lang, aber es ist einfach eine enorm spannende Zeit. Bedenken Sie: Vor ein paar Jahren wäre unser kompletter Ansatz so noch gar nicht möglich gewesen, die Methoden haben sich gewaltig weiterentwickelt. Die Biologie ist jetzt an einem Punkt, an dem die Astronomie im 17. Jahrhundert mit solchen Helden wie Kepler und Newton oder Brahe war. So wie es damals darum ging, die Gesetze der Laufbahn von Planeten zu erklären, wollen wir die Laufbahn von Zellen erforschen. Das ist eine große Aufgabe. Und von ähnlicher Bedeutung.
Zum Weiterlesen:
Einzelzellanalyse - Ein Puzzle mit 37 Trillionen Einzelteilen
Leser:innenkommentare